Литотомическое положение на операционном столе
Обновлено: 18.05.2024
Нет сомнения в том, что за последние десятилетия самой масштабной технологической разработкой стал хирургический робот Da Vinci, который расширяет как географическую, так и хирургическую области применения [1]. Число робот-ассистированных (РА) вмешательств за 2018 г. превысило 1 млн и неуклонно растет.
Использование робота в хирургической практике имеет ряд преимуществ по сравнению с открытым доступом, включая следующие:
1. 3D-изображение высокой четкости (HD) с интегрированным освещением, системой управления фокусом и автоматическим определением оперативного поля, обеспечивающее лучшую визуализацию анатомических структур в ходе операции.
2. Роботические руки, масштабируя и преобразуя движения кистей оперирующего хирурга, позволяют производить прецизионные и маневренные действия, что дает возможность оперировать в трудоемких пространствах, доступных зачастую лишь при открытой хирургии [2].
3. Минимизация прямого контакта с пациентом позволяет снизить риск передачи гематогенных инфекций.
4. Использование робота упрощает оперативные вмешательства у пациенток с ожирением [3—5].
5. Эргономика роботической установки позволяет снизить нагрузку на скелетно-мышечную систему хирурга, особенно при продолжительных операциях [6, 7].
Апикальная поддержка является ключевой в хирургической коррекции пролапса тазовых органов [8]. Сакрокольпопексия (SCP) сохраняет статус «золотого стандарта» при лечении пациенток с апикальным пролапсом гениталий [9]. Данная операция анатомически и патогенетически обоснованна за счет обеспечения I и II уровней поддержки тазового дна по классификации DeLancey [10]).
SCP была впервые представлена в Париже абдоминальным доступом в 1957 г. С 90-х годов XX века данная операция адаптирована под мини-инвазивный доступ A. Wattiez [11] — она объединила высокую эффективность промонтофиксации с преимуществами лапароскопии. Однако данный доступ при выполнении SCP имеет ряд таких недостатков, как длительная «кривая обучения» [12], лимитированный объем движений рук хирурга и тактильного восприятия. Все это может приводить к увеличению продолжительности операции, что негативно влияет на ее широкое внедрение. Роботохирургия наиболее приемлема для проведения SCP ввиду необходимости работы в труднодоступных пространствах малого таза, наложения большого количества швов и продолжительности операции.
Показания к SCP: изолированный апикальный пролапс тазовых органов II—IV стадии по классификации Pelvic Organ Prolapse Quantification (POP-Q) или таковой в сочетании с ректоцеле. Данная операция наиболее предпочтительная у молодых и активных в половом поведении женщин, поскольку использование вагинальных синтетических протезов в подобной ситуации сопряжено с высоким риском формирования mesh-ассоциированных осложнений [13].
Хирургическая техника роботической сакрокольпопексии. Литотомическое положение пациентки на операционном столе. Катетеризация мочевого пузыря катетером Фолея. Правосторонний боковой «докинг» при данной операции предпочтителен, так как обеспечивает доступ ассистенту для выполнения манипуляций вагинальным доступом, а также со стороны дополнительного ассистентского порта в левой подвздошной области.
Размещение троакаров на расстоянии 8 см друг от друга направлено на достижение максимальной амплитуды движений роботических «рук» и предотвращение их интраоперационного «конфликта». Используются оптический троакар (12 мм) и 4 дополнительных троакара (3 из них диаметром 8 мм и один ассистентский троакар диаметром 11 мм). Оптический троакар устанавливается в точке на 2 см выше пупочного кольца. Первые два роботических троакара располагаются латеральнее оптического на расстоянии как минимум 8 см друг от друга во избежание последующей коллизии механизмов. Третий роботический, а также лапароскопический ассистентский порты устанавливаются согласно предыдущему правилу, формируя латинскую букву W (рис. 1).

Рис. 1. Расположение портов при робот-ассистированной сакрокольпопексии.
О — оптический троакар; 1, 2, 3 — дополнительные роботические троакары; А — ассистентский троакар.
Для операции используются следующие инструменты: биполярный зажим, ножницы с возможностью применения монополярного разрезания и коагуляции, атравматичный окончатый зажим, два иглодержателя, один из которых имеет лезвия в основании бранш (рис. 2). Для ассистенции вагинальным доступом применяются вагинальный зонд или маточный манипулятор (рис. 3).

Рис. 2. Набор инструментов для проведения робот-ассистированной сакрокольпопексии.

Рис. 3. Спектр манипуляторов для вагинальной ассистенции при робот-ассистированной сакрокольпопексии.
Выделяют следующие хирургические этапы робот-ассистированной сакрокольпопексии (RA SCP) (рис. 4 на цв. вклейке).

Рис. 4. Этапы выполнения робот-ассистированной сакрокольпопексии.
а — вскрытие париетальной брюшины с мобилизацией передней стенки влагалища и мочевого пузыря; б — вскрытие париетальной брюшины дугласова пространства с мобилизацией промежностного тела и мышц, поднимающих задний проход; в — вскрытие париетальной брюшины в проекции продольной пресакральной связки; г — фиксация передней части сетчатого протеза к передней стенке влагалища; д — фиксация задней части сетчатого протеза к промежностному телу; е — фиксация протеза к продольной пресакральной связке в области крестцового мыса.
I этап. Широко вскрывают париетальную брюшину дугласова пространства, разрез продлевают справа, медиальнее брыжейки сигмовидной кишки до проекции продольной пресакральной связки на уровне крестцового мыса (см. рис. 4в на цв. вклейке). Предварительная идентификация анатомических ориентиров позволяет обезопасить ход операции (правый мочеточник, правые общая и внутренняя подвздошные артерии, срединная сакральная артерия и вена). Затем тупым путем производят диссекцию ректовагинального клетчаточного пространства с целью выделения средних порций лобково-прямокишечных мышц и ректовагинальной перегородки до уровня промежностного тела (см. рис. 4б на цв. вклейке). После вскрытия пузырно-маточной складки переднюю стенку влагалища отделяют от задней стенки мочевого пузыря до уровня его шейки с обязательным сохранением целостности лобково-шеечных связок (см. рис. 4а на цв. вклейке). При наличии тела матки после данного этапа предпочтительно выполнение супрацервикальной гистерэктомии с формированием культи шейки матки монофиламентными узловыми швами.
II этап. Из полипропиленового материала с индексом soft выкраивают 2 лоскута особой формы: задний размерами 15×8 см, передний — 5×3 см (рис. 5). Нерассасывающимся плетеным шовным материалом (Ethibond) края первого лоскута фиксируют к средней порции лобково-прямокишечных мышц (пучок мышц, поднимающих задний проход) с обеих сторон, а также к промежностному телу (см. рис. 4д на цв. вклейке). При этом фиксацию выполняют на глубину до 5 мм в связи с риском травматизации полового нерва, который располагается в области проекции наружной стенки седалищно-прямокишечной ямки в расщеплении фасции внутренней запирательной мышцы (канал Алькока). Край первого лоскута после предварительной идентификации мочеточников также фиксируют к крестцово-маточным связкам и задней поверхности шейки матки или куполу влагалища. Фиксацию края второго лоскута выполняют к передней стенке влагалища (см. рис. 4г на цв. вклейке), передней поверхности культи шейки матки или куполу влагалища, а также к первому лоскуту отдельными нерассасывающимися лигатурами. Расстояние между швами на передней и задней стенках влагалища должно составлять 2,5 см и 3,5 см соответственно.

Рис. 5. Задний и передний лоскуты протеза, используемые при сакрокольпопексии.
III этап. Свободный конец заднего лоскута в состоянии умеренного натяжения фиксируют нерассасывающимся шовным материалом к продольной пресакральной связке (см. рис. 4е на цв. вклейке), в результате чего протез приобретает Y-образную форму (рис. 6).

Рис. 6. Конечный вид протеза при сакрокольпопексии.
1 — крестец, 2 — сетчатый протез, 3 — влагалище.
IV этап. Производят перитонизацию сетчатого протеза непрерывным рассасывающимся швом, обеспечивая его ретроперитонеальное расположение. По окончании операции обязательно проведение тампонады влагалища марлей, смоченной антисептическим раствором.
Субъективное улучшение оценено при помощи специальных анкет: PFDI-20 (Pelvic Floor Distress Inventory), PFIQ-7 (Pelvic Floor Impact Questionnaire) и PISQ-12 (Pelvic Organ Prolapse/Urinary Incontinence Sexual Questionnaire). Отличный и хороший субъективный результат, отраженный улучшением результатов прохождения опросников, отметили 70 (94,6%) пациенток.
Оценка анатомических результатов проводилась путем вагинального осмотра с применением системы POP-Q. У 61 (82,4%) пациентки отмечен хороший и отличный результат операции, заключающийся в отсутствии рецидива пролапса или наличии такового I стадии. Однако у 13 (17,6%) женщин выявлен рецидив опущения половых органов II—III стадии, проявившийся исключительно в форме цистоцеле. Только 2 (2,7%) больных была произведена хирургическая коррекция пролапса повторно (SCP и вагинальная кольпопексия системой OPUR).
Заключение
Робот-ассистированная сакрокольпопексия — это операция выбора у живущих половой жизнью женщин с апикальным пролапсом гениталий. Использование робота в хирургической практике приоритетно у пациенток с ожирением, выраженным спаечным процессом, а также с рецидивными формами пролапса гениталий после коррекции опущения тазовых органов сетчатыми протезами как вагинальным, так и лапароскопическим доступами.
Трансанальная доплер-контролируемая дезартеризация геморроидальных узлов с мукопексией
Трансанальная доплер-контролируемая дезартеризация геморроидальных узлов (HAL) – это вмешательство, при котором ультразвуковым датчиком определяется положение ветвей артерии, снабжающей кровью нижний отдел прямой кишки, которые выше зубчатой линии прошиваются и перевязываются с целью прекращения притока крови к слизистой оболочке в зоне образования геморроидальных узлов [1].
Трансанальная доплер-контролируемая дезартеризация геморроидальных узлов при геморрое третьей и четвертой степени может быть дополнена методикой мукопексии (RAR) - прошиванием нитью провисающей слизистой оболочки и подтягивание прошитой ткани вверх с целью подтяжки пролапса слизистой прямой кишки [2].
Коды МКБ-10
| МКБ-10 | |
| Код | Название |
| К64 | Геморрой и перианальный венозный тромбоз |
| К64.0 | Геморрой первой степени |
| К64.1 | Геморрой второй степени |
| К64.2 | Геморрой третьей степени |
| К64.3 | Геморрой четвертой степени |
| К64.8 | Другой уточненный геморрой |
| К64.9 | Неуточненный геморрой |
Дата разработки протокола: 2018 год.
Сокращения, используемые в протоколе:
| ИФА | – | Иммуноферментный анализ |
| ВИЧ | – | Вирус ммунодефицита человека |
| HAL | – | Лигирование геморроидальных артерий (Hemorrhoidal Artery Ligation) |
| RAR | – | Ректоанальное восстановление (мукопексия) (Recto Anal Repair) |
Пользователи протокола: хирурги, колопроктологи, анестезиологи-реаниматологи, средние медицинские работники.
Категория пациентов: взрослые.

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной

13-15 октября, Алматы, "Атакент"
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
- трансанальная доплер-контролируемая дезартеризация геморроидальных узлов (при геморрое первой и второй степени);
- трансанальная доплер-контролируемая дезартеризация геморроидальных узлов с мукопексией (при геморрое третьей и четвертой степени).
Диагностика
Перечень основных и дополнительных диагностических мероприятий
Основные диагностические мероприятия
(имеющие 100% вероятность применения):
- колоноскопия или аноскопия/ректороманоскопия (исключить/выявить источник кровотечения, наличие новообразований);
- консультация анестезиолога-реаниматолога.
Дополнительные диагностические мероприятия (менее 100% вероятности применения):
- общий анализ крови;
- коагулограмма крови;
- биохимический анализ крови;
- ИФА на ВИЧ;
- ИФА на гепатиты В и С;
- анализ крови RW (реакция Вассермана);
- группа крови, резус фактор;
- ирригоскопия/ирригография (при подозрении на наличие хронического копростаза).
Лечение
Цель проведения вмешательства:
- лигирование терминальных ветвей верхней прямокишечной артерии;
- подтяжка слизистой терминального отдела прямой кишки.
Показания к вмешательству:
- неэффективность консервативной терапии при любой стадии геморроидальной болезни.
Противопоказания к вмешательству:
- острый тромбоз геморроидальных узлов;
- сопутствующие заболевания анального канала (трещина, свищ, парапроктит и т.д.);
- воспалительные заболевания толстой кишки (болезнь Крона, язвенный колит в период обострения и т.д.);
- гематологические заболевания (анемия средней и тяжелой степени тяжести, лейкозы, лимфогранулематоз, злокачественные заболевания крови, коагулопатии различного генеза);
- острые соматические состояния (сепсис, шок, инфаркт миокарда, острое нарушение мозгового кровообращения);
- злокачественные опухоли;
- тяжелые иммунодефицитные состояния;
- пациенты, принимающие антикоагулянты (во время проведения вмешательства необходимо временно приостановить прием антикоагулянтов);
- беременность и детский возраст.
Требования к проведению вмешательства
Квалифицированный персонал:
- хирурги (не ниже первой квалификационной категории, с опытом проведения подобных вмешательств не менее 10 процедур под наблюдением эксперта);
- колопроктологи (не ниже второй квалификационной категории).
Условия для проведения вмешательства:
Трансанальная доплер-контролируемая дезартеризация геморроидальных узлов с мукопексией проводится согласно Санитарным правилам «Санитарно-эпидемиологические требования к объектам здравоохранения» в медицинских учреждениях:
- оказывающих стационарозамещающую хирургическую помощь;
- оказывающих стационарную хирургическую помощь.
Требования к расходным материалам [3]:
- стерильный одноразовый аноскоп (ректоскоп) с ультразвуковым датчиком для доплерометрии и c подсветкой;
- стерильный атравматический шовный материал;
- стерильный перевязочный материал.
Требования к оснащению [3]:
- стерильный доплер-операционный комплекс в комплекте;
- звуковое устройство с динамиком (спикер), имеющий связь с доплер-операционным комплексом;
- стерильный иглодержатель;
- стерильный проталкиватель узлов.
Подготовка пациента к проведению операции [4]:
- пациенту назначается прием осмотических слабительных препаратов за 1 сутки до операции или выполнение очистительных клизм для полного очищения кишечника перед операцией (за 2-3часа);
- по рекомендации анестезиолога/реаниматолога назначаются седативные препараты;
- за 20-30 минут до операции проводится антибактериальная профилактика внутримышечным или внутривенным введением антибактериального препарата (цефалоспорины II, III поколения);
- необходимо выбрить и обработать перианальную зону антисептиком, не содержащим спирта;
- больного укладывают на операционный стол, в положении на спине ему раздвигают ноги и фиксируют. Наиболее удобным положением для пациента является положение, как для промежностного камнесечения (см. рис. 1). При этом, таз пациента должен быть приподнят и слегка выдвинут кпереди за край стола, головной конец стола должен быть слегка приподнят и снабжен мягкой подушкой для головы пациента, операционное поле должно быть отграничено стерильным бельем;
- общая проводниковая, перидуральная или спиномозговая анестезия; тотальный эндотрахеальный наркоз.

Рисунок 1. Литотомическое положение пациента на операционном столе [5].

Рисунок - 2. a) определение локализации и b) прошивание и перевязка геморроидальных артерий при помощи аноскопа с доплеровским датчиком [6].
Далее, аноскоп поворачивают для обнаружения проекции других оставшихся геморроидальных артерий (в среднем от 5 до 8), которые лигируют аналогичным образом. Операцию завершают контролем гемостаза 8.
Вариант 2. Техника проведения трансанальной доплер-контролируемой дезартеризации геморроидальных узлов с мукопексией:
В случае хронического геморроя третьей и четвертой степени с пролапсом слизистой вместе с геморроидальными узлами ниже анального кольца операцию на начальном этапе выполняют аналогично варианту 1 техники проведения трансанальной доплер-контролируемой дезартеризации геморроидальных узлов. В последующем проводят мукопексию при помощи аноскопа путем наложения «якорного» шва с захватом мышечного слоя стенки прямой кишки на глубине 4-6 см от зубчатой линии. Далее, используя лигатуру «якорного» шва, в направлении зубчатой линии (не доходя до последней 0,5-0,8 см) с захватом слизистой накладывают непрерывный обвивной шов (от 4 до 8 стежков) на дилатированную сосудистую ткань геморроидального сплетения. Концы нити подтягивают, и собирая слизистую в складки, завязывают (смотрите рисунок 3). Аналогичную технику применяют в других проекциях, где имеется пролабирование слизистой оболочки прямой кишки. Операцию завершают контролем гемостаза [6,8].

Рисунок - 3. a) пролабирующий геморроидальный узел b) мукопексия непрерывным обвивным швом и подтяжка слизистой прямой кишки [6].
Рекомендации послеоперационного периода:
- при обезболивании назначают ненаркотические анальгетики;
- после операции в течение нескольких дней исключить из рациона острую пищу, а также алкогольные напитки;
- диета должна быть направлена на формирование мягкого кашицеобразного или полужидкого стула;
- не рекомендуется тяжелая физическая нагрузка (до 20 дней);
- не рекомендуется тепловые процедуры (сауна, баня, горячая ванная) (до 14 дней);
- не рекомендуется половой контакт (7-10 дней);
- исключить самостоятельные манипуляции в области операции (клизмы, введение свечей).
Информация
Источники и литература
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1). Баймаханов Болатбек Бимендеевич – председатель правления АО «Национальный научный центр хирургии им. А.Н. Сызганова», доктор медицинских наук, профессор.
2). Абдуллаев Марат Шадыбаевич – председатель союза врачей-колопроктологов Республики Казахстан, доктор медицинских наук, профессор.
3). Шакеев Кайрат Танабаевич – заведующий кафедрой хирургических болезней №1 РГП на ПХВ «Карагандинский государственный медицинский университет», доктор медицинских наук, профессор.
4). Медеубеков Улугбек Шалхарович – заместитель председателя правления АО «Национальный научный центр хирургии» им. А.Н. Сызганова» по научно-клинической и инновационной деятельности, доктор медицинских наук, профессор.
5). Тян Леонид Владимирович – руководитель центра амбулаторной колопроктологии ГКП на ПХВ «Городская больница №1» Управления здравоохранения Акимата города Астаны, кандидат медицинских наук.
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
1). Царьков Петр Владимирович – директор клиники колопроктологии и малоинвазивной хирургии Первого Московского государственного медицинского университета им. И.М. Сеченова, доктор медицинских наук, профессор.
2). Ингрид Хаунольд – руководитель «Центра хирургии тазового дна» больницы Сестер Милосердия города Вена (Австрия), доктор медицины, профессор.
Указание условий пересмотра протокола: Пересмотр протокола через 5 лет и/или при появлении новых методов диагностики/ лечения с более высоким уровнем доказательности.
Операция при раке простаты
Операция при раке простаты – лечение опухолевого процесса предстательной железы методом ее удаления. Данный вид лечения мы выполняем в тех случаях когда раковый процесс не распространился за пределы предстательной железы (стадии Т1 и Т2). В некоторых случаях операция при раке простаты выполняется и при более распространенных стадиях.
Основная операция, выполняемая при раке простаты, – это радикальная простатэктомия выполняемая открытым или лапароскопическим способом. В данной статье речь пойдет об открытой методике выполнения удаления предстательной железы.
Во время операции врач удаляет всю предстательную железу и окружающие ее ткани, в том числе и семенные пузырьки, а если необходимо, и местные лимфатические узлы.
В настоящее время мы применяем следующие техники операции при раке простаты:
- Открытая радикальная простатэктомия;
- Малоинвазивная лапароскопическая простатэктомия;
- Нерво-сберегающая радикальная простатэктомия.
Так же может проводиться трансуретральная резекция простаты при опухоли предстательной железы. Данный вид лечения выполняется как вынужденный для облегчения симптомов заболевания.
На выбор способа хирургического вмешательства влияет ряд факторов:
- Стадия рака простаты, т.е. размер опухоли и ее распространенность;
- Степень рака простаты, т.е. его агрессивность;
- Прогноз рака простаты;
- Выраженность симптомов заболевания;
- Возраст мужчины;
- Общее состояние организма мужчины и наличие сопутствующих заболеваний.
В данной статье мы расскажем все про предоперационную подготовку, анестезию и технику выполнения открытой радикальной простатэктомии. Информацию о малоинвазивной лапароскопической и робот-ассистированной радикальной простатэктомии вы найдете в этой статье.
Подготовка перед операцией по поводу рака простаты
Предоперационная подготовка включает в себя ряд важных аспектов.
Перед операцией вам необходимо сдать ряд анализов: общий анализ крови и мочи, биохимический анализ крови, анализ на свертывающую систему крови. Также в стандартное предоперационное обследование входят ЭКГ и рентген грудной клетки. При необходимости назначаются и другие обследования. По результатам общего осмотра и медицинского обследования врач сможет оценить вашу готовность к операции. Анализы сдаются в амбулаторных условиях за 1-2 недели до операции.
Если у вас есть склонность к кровоточивости или вы принимаете препараты разжижающие кровь, такие как аспирин, варфарин и др., на предварительной консультации вы должны обязательно поставить в известность вашего врача. За одну-две недели до операции необходимо прекратить прием этих препаратов.
Госпитализация в стационар происходит за один-два дня до операции.
Накануне операции с вами побеседует хирург и анестезиолог. Врачи в подробностях объяснят вам все, что будет происходить во время анестезии и операции, расскажут о возможных рисках и осложнениях хирургического вмешательства и анестезии. В процессе беседы вы сможете задать врачам любые интересующие вас вопросы. По окончании беседы вам необходимо будет подписать информированное согласие на анестезию и операцию.
Большое значение имеет подготовка кишечника к операции. За 24 часа до операции врач посоветует принимать только жидкую пищу. Очистительная клизма выполняется вечером накануне и утром перед операцией.
Кроме того, не забывайте, что если хирургическое вмешательство выполняется под общей анестезией, то последний прием пищи разрешается вечером накануне операции. В день операции не разрешается ни есть, ни пить. При необходимости приема лекарств, их можно запить небольшим глотком воды.
За месяц до операции по удалению рак простаты мужчина должен начать тренировать мышцы тазового дна.
Упражнение Кегеля для укрепления мышц тазового дна состоит из трех частей (медленного сжатия, сокращения и выталкивания). Перед началом упражнения необходимо расслабить живот и ягодицы. Далее напрягите мышцы тазового дна, как при остановке дефекации. При этом вы должны чувствовать, сжатие анального отверстия. Удерживайте такое напряжение в течение 3-5 секунд. По истечении времени расслабьтесь. Это упражнение сжатия. Упражнение по сокращению заключается в быстром напряжении и расслаблении мышц промежности. И третья группа упражнений – это выталкивание. При выполнении этого упражнения необходимо потужиться, как при дефекации или мочеиспускании.
Каждая часть выполняется по 5-10 раз, упражнение Кегеля повторяется 3-5 раз в день. Каждую неделю необходимо увеличивать частоту выполнения каждой части упражнения на 5 раз, а упражнение делать не менее 5 раз в день. Сначала выполняйте упражнение Кегеля лежа, позже вы сможете делать его сидя или стоя.
Операция при раке простаты выполняется под комбинированной анестезией
Радикальная простатэктомия может выполняться под общей или регионарной (спинальной или эпидуральной) анестезией. Каждый вид анестезии имеет свои преимущества и недостатки. Большинство анестезиологов предпочитают выполнять спинальную или эпидуральную анестезию, так как она ассоциировано с меньшим числом интра- и посленаркозных осложнений. Кроме того постановка эпидурального катетера позволяет обеспечить эффективное послеоперационное обезболивание. Регионарные методы анестезии подразумевают тот факт, что мужчина находится в сознании весь период операции. Для предотвращения психо-эмоционального стресса анестезиолог может дополнять регионарную анестезию введением седативных препаратов.
В случае невозможности использования регионарных методов обезболивания, операция при раке простаты выполняется под общей эндотрахеальной анестезией. В этом случае весь период операции пациент находится без сознания, а дыхание осуществляется через специальную трубку при содействии аппарата искусственной вентиляции.
Радикальная простатэктомия
Открытая радикальная простатэктомия может выполняться из двух доступов:
- Открытая радикальная позадилонная простатэктомия;
- Открытая радикальная перинеальная простатэктомия;
Открытая радикальная позадилонная простатэктомия
Позадилонная простатэктомия – хирургическая методика удаления простаты через разрез в области живота. Методика позволяет удалять предстательную железу больших размеров, параллельно могут удаляться регионарные лимфатические узлы.
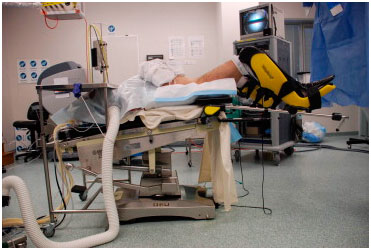
Операция выполняется в положении пациента на спине или, так называемой, нижней литотомической позиции (на спине, с ногами, установленными на специальные подставки).
После оказания анестезиологического пособия хирург приступает к обработке операционного поля антисептиками и обкладыванию зоны операции стерильным бельем. Далее хирург выполняет нижний срединный разрез длиной 7-9 см, как показано на рисунке.
Далее послойно рассекаются ткани передней стенки живота, хирург выделяет шейку мочевого пузыря, предстательную железу и крупные подвздошные сосуды, вдоль которых располагаются местные (тазовые лимфатические узлы).
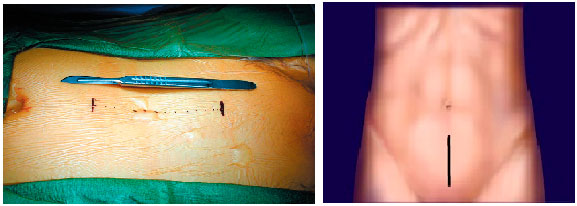
При необходимости перед простатэктомией может проводиться и лимфаденэктомия – удаление регионарных лимфатических узлов. Лимфаденэктомия всегда выполняется до удаления простаты. Далее хирург производит мобилизацию и резекцию простаты с расположенными рядом с ней семенными пузырьками. При удалении простаты пересекается мочеиспускательный канал, простатическая часть уретры удаляется вместе с предстательной железой. После удаления простаты хирург сшивает оставшуюся часть уретры с шейкой мочевого пузыря – т.е. накладывается везико-уретральный анастомоз. В этот момент в мочевой пузырь заводится катетер. После осуществления гемостаза и дренирования ложа простаты (постановки дренажа), операционная рана послойно ушивается. Кровопотеря при такой операции составляет около 200-300 мл.
Длительность операции составляет 2,5-3,5 часа.
Описание операции выглядит довольно просто. Однако на самом деле операция при раке простаты это довольно сложная хирургическая процедура урологии. Мы выполняем данную операции в очень больших количествах и имеем довольно богатый практический опыт, ведь в России радиальная простатэктомия впервые была выполнена в НИИ Урологии. И все же, более тонкие возможности сохранения нервных волокон для функции эрекции, полное сохранение аппарата удерживающего мочу, сокращение послеоперационного периода, снижение болевых ощущений и многие другие важные аспекты для сохранения высокого качества жизни больного – все это требует постоянного совершенствования навыков.
Открытая радикальная перинеальная простатэктомия
Открытая промежностная (перинеальная) простатэктомия – хирургическая техника, позволяющая удалить простату через разрез в области промежности. Впервые операция была внедрена в 1869 году Бюхлером, и оставалась методом выбора хирургического лечения рака простаты вплоть до 70-ых годов, когда была разработана методика простатэктомии позадилонным доступом. Позадилонная простатэктомия приобрела популярность за счет того, что она давала возможность выполнять удаление лимфатических узлов. Промежностный доступ обладает рядом преимуществ, по сравнению с позадилонным доступом: более короткий период операции, более легкий доступ к простате, меньший объем кровопотери, менее выраженный болевой синдром в послеоперационном периоде, более короткий срок госпитализации и восстановления. Промежностный доступ подходит для мужчин с ожирением. Недостатком является невозможность удаления местных лимфатических узлов, что требует выполнение лапароскопии. Кроме того данная техника не позволяет хирургу аккуратно работать с нервными волокнами, которые расположенны рядом с простатой и ответственны за потеную. Данный факт не дает возможность выполнить нерво-сберегающую простатэктомию.
Операция промежностным доступом НЕ может выполняться в случае: анкилозов, тяжелых артритов суставов таза, наличия искусственных протезов. Это затрудняет правильную укладку пациента на операционном столе. Кроме того, выполнение промежностной простатэктомии затруднено при большом размере простаты. В этом случае может проводиться позадилонная простатэктомия или же перед операцией назначается гормональная терапия для уменьшения простаты в размере.

Открытая промежностная простатэктомия выполняется в верхнем литотомическом положении, как показано на рисунке. Пациент лежит на спине с ногами согнутыми в коленях и расположенных в специальных подставках – «стременах».
После укладки пациента на столе хирург обрабатывает операционное поле антисептическими йод- или спиртсодержащими препаратами.
Далее зона операции обкладывается стерильным бельем, хирург выполняет U-образный разрез в области промежности (область, расположенная между мошонкой и анусом).
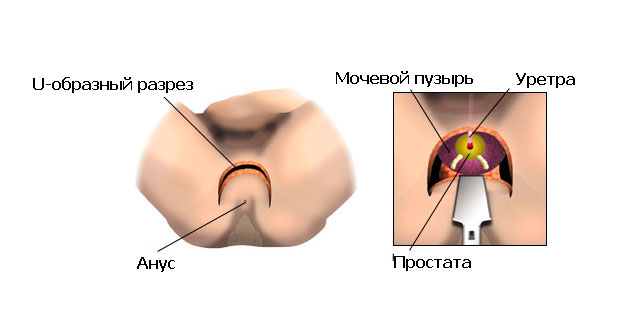
После послойного рассечения тканей и визуализации предстательной железы и семенных пузырьков, хирург приступает к их удалению. Простата удаляется вместе с расположенной в ней простатической частью уретры, после чего оставшийся участок мочеиспускательного канала сшивается с шейкой мочевого пузыря. В мочевой пузырь вводится катетер. Рана ушивается послойно.
Длительность операции 2-2,5 часа.
Нерво-сберегающая простатэктомия
Данная операции при раке простаты позволяет предупредить нарушение после оперативного вмешательства. Процесс эрекции контролируют два нервных пучка, проходящих вдоль простаты. Во время нерво-сберегающей простатэктомии хирург максимально пытается сохранить целостность этих нервов. Однако не всегда существует возможность удаления простаты без повреждения нервов. В этом случае риск нарушения эректильной дисфункции намного выше. Выполнение нерво-сберегающей операции при раке простаты ассоциировано с риском того, что часть раковых клеток останется в области сохраненных нервов. Поэтому возможность выполнения нерво-сберегающей техники оценивается во время проведения операции. Хирург визуально оценивает вовлечение сосудисто-нервных волокон в опухолевый процесс. При вовлечении последних, даже несмотря на просьбы пациента, о сохранении функции эрекции хирург удаляет сосудисто-нервные пучки. Такая техника оправдывается тем, что онкологических результат гораздо важнее, а эректильная функция, при желании, может быть восстановлена применением протеза.
В некоторых случаях мы сохраняем сосудисто-нервные пучки с одной стороны если по данным биопсии простаты и визуально во время операции нет вовлечения нервных волокон в раковый процесс. При таком подходе шансы сохранения естественной потенции гораздо выше.
Нерво-сберегающая простатэктомия подходит для мужчин с раком простаты на ранней стадии в том случае когда опухоль предстательной железы полностью ограничена железой. Если опухоль располагается в непосредственной близости к нервам или прорастает в них, выполнение нерв-сберегающей простатэктомии невозможно.
После операции при раке простаты
После операции на мобильной кровати вас транспортируют в палату интенсивной терапии. В первые несколько часов врач будет пристально наблюдать за течением раннего послеоперационного периода (частотой сердечных сокращений, артериальным давлением, дыханием, восстановлением сознания).
Более подробную информацию о том что будет происходить с вами после операции по поводу рака простаты вы сможете ознакомиться в статье: После операции.
Осложнения радикальной простатэктомии
- Сужение шейки мочевого пузыря в области везико-уретрального анастомоза, в последующем приводящее к нарушению мочеиспускания. В 2,8% случаев у мужчин наблюдается сужение шейки мочевого пузыря после радикальной простатэктомии.
- Редко радикальная операция при раке простаты осложняется повреждением уретры или прямой кишки.
- Формирование тромбов в глубоких венах нижних конечностей в раннем послеоперационном периоде может приводить к такому тяжелому последствию как ТЕЛА (тромбоэмболия ветвей легочной артерии). Раннее возобновление подвижности, использование компрессионных бинтов помогают снизить риск тромботических осложнений.
- Расхождение швов, нагноение раны и генерализованная инфекция – редкие осложнения радикальной простатэктомии.
Побочные эффекты операции при раке простаты
После операции при раке простаты возможно развитие следующих побочных эффектов: недержание мочи и нарушение функции эрекции. Эти побочные эффекты в настоящее время встречаются довольно редко, по сравнению с прошлым. А выполнение нерво-сберегающей операции при раке простаты значительно снижает риск развития импотенции.
После радикальной простатэктомии мужчины могут испытывать только сухой оргазм, т.е. не происходит выделения эякулята. Это связано с тем, что основные источники семенной жидкости (простата и семенные пузырьки) удаляются во время операции, а семявыносящий проток «отключается» от мочеиспускательного канала. Однако отсутствие эякуляции не влияет на ощущения, испытываемые мужчиной во время оргазма.
Удаление мочевого пузыря
Инвазивный рак мочевого пузыря – это опухоль, которая распространяется глубже слизистой оболочки мочевого пузыря, поражая подслизистый и мышечный слои (стадия Т2 и выше).
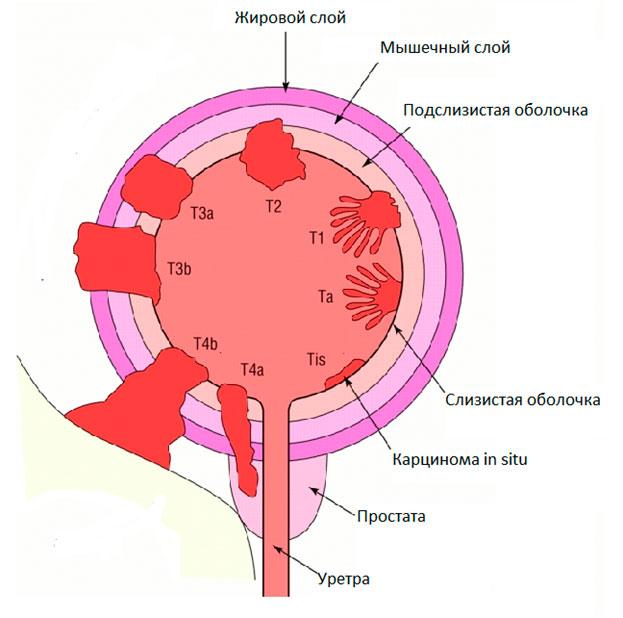
Рисунок. Стадии рака мочевого пузыря.
Инвазивный рак мочевого пузыря требует более интенсивного лечения. Удаление мочевого пузыря с расположенными рядом лимфатическими узлами и органами является оптимальным лечением, позволяющим прогнозировать лучшую курабельность злокачественного процесса и добиться низкого риска рецидива. Такая операция носит название радикальной цистэктомии. При радикальном удалении мочевого пузыря и лимфоузлов у мужчин удаляются также простата и семенные пузырьки, а у женщин мочеиспускательный канал, матка и придатки, передняя стенка влагалища.

Рисунок. Радикальное удаление мочевого пузыря у женщин (зеленым обозначены органы, подлежащие удалению).
Рисунок. Радикальное удаление мочевого пузыря у мужчин (зеленым обозначены органы, подлежащие удалению).
Показания для удаления рака мочевого пузыря
- Инвазивный рак без метастазов, или с регионарными метастазами, поддающимися хирургическому удалению;
- Поверхностный рак мочевого пузыря, характеризующийся следующим: 1. неоднократное развитие рецидивов после трансуретральной резекции, интравезикальной химио- или иммунотерапии; 2. поражение большой поверхности мочевого пузыря; 3. распространение рака на простатическую часть уретры;
- рак in situ (CIS), или плоский рак, не поддающийся интравезикальной иммунотерапии или химиотерапии;
- Рак на ранней стадии (Т1), но низкодифференцированный, т.е. с высоким риском рецидива (степень 3);
- Паллиативная мера при раке на поздних стадиях, с целью облегчения боли, устранения симптомов повреждения мочевого пузыря (учащенное мочеиспускание, кровотечения и др.);
- Первичная аденокарцинома, сквамозно-клеточная карцинома или саркома.
Что такое нервосберегающая операция удаления мочевого пузыря?
Удаление простаты и семенных пузырьков в сочетании с цистэктомией часто приводит к повреждению сосудисто-нервных пучков, ответственных за работу половой системы. Это может приводить к импотенции после удаления пузыря. Мужчины с хорошей эректильной функцией, которые желают сохранить свою потенцию после радикальной цистэктомии могут быть кандидатами на операцию с сохранением пещеристых нервов, подобную той, что выполняется при нервосберегающей радикальной простатэктомии.
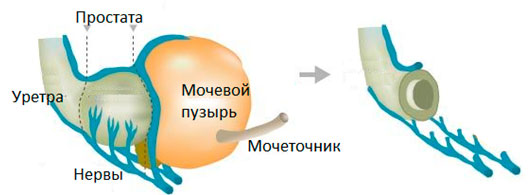
Рисунок. Нервосберегающее удаление мочевого пузыря.
Нервосберегающая цистэктомия сопряжена с риском неполного удаления всех злокачественных тканей, что подвергает пациента более высокому риску рецидива. Таким образом, отбор пациентов является критическим при выполнении нервосберегающей цистэктомии. Сохранение нервов с одной стороны может рассматриваться у пациентов с инвазивной опухолью на задней, боковой или тригональной области мочевого пузыря. Двусторонняя нервосберегающая операция может быть выполнена у пациентов с неинвазивным раком или инвазивной опухолью на передней стенке или куполе мочевого пузыря.
Химиотерапия и облучение перед удалением мочевого пузыря
Курс химиотерапии и облучения могут проводиться перед удалением мочевого пузыря с целью уменьшения размера опухоли и выполнения максимально органосохраняющей операции.
Неоадъювантная химиотерапия с последующей радикальной цистэктомией в настоящее время находит широкое применение и в скором времени станет стандартом лечения инвазивного рака мочевого пузыря. Несколько исследований показали более высокую выживаемость пациентов, у которых радикальной цистэктомии предшествует неоадъювантная химиотерапия, особенно для пациентов с Т3, Т4 стадией.
Исследования свидетельствуют, что предоперационная лучевая терапия не улучшает исход заболевания у пациентов, перенесших цистэктомию. Кроме того, предоперационная лучевая терапия увеличивает риск хирургических осложнений и делает создание нового мочевого резервуара с использованием облученного кишечника более трудной. Поэтому радиотерапия больше не используется регулярно.
Подготовка к удалению мочевого пузыря
Удаление мочевого пузыря серьезное хирургическое вмешательство, требующее тщательной предоперационной подготовки.
Перед удалением мочевого пузыря требуется пройти всестороннее обследование и максимально "оптимизировать" состояние здоровья.
Если вы страдаете артериальной гипертензией, диабетом, анемией и др., вам необходимо посетить вашего лечащего врача, чтобы убедиться, что ваша болезнь компенсирована.
Откажитесь от алкоголя и курения как минимум за месяц до лечения! Это улучшит ваше общее состояние и снизит риск осложнений анестезии.
Еще один важный аспект подготовки – это очищение кишечника. В процессе операции он будет использоваться для создания новых путей оттока мочи, поэтому важно, чтобы он был максимально очищен. За три дня до операции необходимо перейти на пищу жидкой или сметанообразной консистенции. За 36 часов до операции рекомендуется употреблять только жидкости (вода, чай, соки и др.), исключая из рациона молочные напитки. За день до операции назначаются специальные слабительные препараты и выполняются клизмы. Очищение кишечника также включает в себя и деконтаминацию, другими словами стерилизацию. Это достигается с помощью приема антибиотиков, которые, действуя в просвете кишечника, уничтожают болезнетворные микроорганизмы.
Если вы принимаете эти препараты: агренокс, плавикс, витамин Е, аспирин, напрксен и др., обязательно сообщите об этом хирургу и анестезиологу. За 7-14 дней до хирургического вмешательства необходимо приостановить их прием для снижения риска кровотечений.
Операции в области таза ассоциированы с высоким риском осложнений тромбоэмболии. Поэтому накануне проводится профилактика с использованием специальных препаратов низкомолекулярных гепаринов.
Накануне лечения необходимо побрить область паха, что обеспечит максимальное соблюдение стерильности.
Накануне и утром в день операции запрещается есть и пить. Несоблюдение данного правила может повлечь за собой серьезные осложнения анестезии.
Анестезия при удалении мочевого пузыря
Удаление мочевого пузыря выполняется под общей анестезией. Весь период операции вы будете находиться без сознания. Искусственная вентиляция легких будет осуществляться с использованием дыхательного аппарата. А все жизненно-важные функции организма будут контролироваться посредством современного оборудования. Дополнительное обезболивание может достигаться с помощью эпидуральной анестезии. Для этого в области спины устанавливается катетер, который позволит контролировать боль не только в процессе хирургического вмешательства, но и несколько дней после него. За оказание анестезиологического пособия отвечает высококвалифицированный врач анестезиолог-реаниматолог. Перед операцией он проведет осмотр и обсудит с вами все детали анестезии. Вы можете узнать у него о возможных побочных эффектах и рисках. После чего необходимо будет подписать согласие на анестезиологическое пособие.
Вечером перед хирургическим вмешательством могут назначаться седативные, успокоительные препараты, что создаст для вас психо-эмоциональный комфорт.
В операционной
Операция начинается с оказания анестезиологического пособия. После того как врач наладит мониторинг всех жизненно важных функций и вы уснете, вас уложат на операционном столе.
Для мужчин используется положение на спине. У женщин модифицированное литотомическое положение: на спине, с ногами, приведенными к туловищу и установленными на специальные подставки.

Рисунок. Положение на спине.

Рисунок. Модифицированное литотомическое положение.
В мочевой пузырь вводится катетер. После подготовки операционного поля выполняется стандартный срединный разрез, от лонного сочленения до пупка или выше, огибая его.

Рисунок. Разрез для удаления мочевого пузыря.
Радикальное удаление мочевого пузыря выполняется с соблюдением следующих принципов:
- Принцип радикализма. Мочевой пузырь и все расположенные рядом ткани и лимфоузлы, куда распространился рак, удаляются единым блоком в пределах здоровой зоны;
- Принцип абластики заключается в максимальном соблюдении мер по предотвращению распространения по организму раковых клеток из раны;
- Принцип антибластики направлен на уничтожение раковых клеток, рассевающихся в ране во время операции. Это может достигаться путем обработки раны 96% спиртом или раствором йода и т.д.
Таким образом, в процессе операции хирург удаляет мочевой пузырь, лимфатические узлы и органы, с соблюдение основных онкологических принципов. Это достаточно длительный процесс, но на этом операция не заканчивается.
Вторым этапом является формирование новых путей оттока мочи. В настоящее время для этого существует множество методик. Об этом вы сможете прочитать в статье "Отведение мочи после удаления мочевого пузыря".
Операция заканчивается послойным ушиванием ран. В ранах оставляются дренажи и катетеры, швы укрываются стерильными повязками.

Рисунок. После удаления мочевого пузыря.
Все удаленные органы и ткани отсылаются на гистологическое исследование.
Когда закончится анестезия, вас транспортируют в палату пробуждения до полного восстановления сознания. После этого вас переведут в общую палату отделения интенсивной терапии. В клинике вам необходимо будет провести не менее семи дней. Более подробную информацию вы сможете прочитать в статье "После операции рака мочевого пузыря".
Фонкус на деталях. Положение больного на операционном столе при антеградном и ретроградном доступе

В 1955 году была описана тенхика чрескожного доступа к почке в положении пациента на спине [1]; около 20 лет спустя была разработана операция чрескожной нефротитрипсии (ЧНЛТ) [2], и впоследствии техника чрескожных манипуляций с камнями была стандартизована [3]. ЧНЛТ, которая до сих пор считается методом выбора для лечения крупных камней почки, была изначально разработана с использованием косого положения больного на спине, но поздее положение на живота стало стандартом. В настоящее время, даже более сложные эндоурологические пособия, например одновременное или последовательное использование чрескожных манипуляций на почке и уретероскопия, продолжают осуществлятся в положении больного на животе, которое считается общепринятым в силу исторических причин 7. Положение на животе, как известно, предоставляет большую площадь поверхности для выбор места пункции, более обширное пространство для манипуляций с инструментами и, возможно, связано с меньшим риском повреждения внутренних органов. Тем не менее, оно имеет несколько недостатков, включая дискомфорт для пациента, увеличенную лучевую нагрузку на хирурга (работающего руками в зоне облучения), необходимость нескольких санитаров для правильного расположения больного перед операцией и для дополнительных интраоперационных изменений положения в случае одновременного инструментального пособия на мочеточнике, более очевидный риск, связанный с точками давления, сердечно-сосудистыми и вентиляционными нарушениями (особенно у больных с морбидным ожирением, аномалиями позвоночника, ослабленных пациентов), эндокринными и фармакокинетическими эффектами 21.
Предлагались различные безопасные и эффективные модификации положения больно при ЧНЛТ, включая положение на животе с раздвинутыми ногами, которое Scarpa с соавт. использовали несколько лет назад, обратное литотомическое положение, положение на боку и положения на спине [7–9,19–25]. В 1987 г. Valdivia-Urìa описал технику ЧНЛТ в положении больного на спине с подушкой объемом 3 л, подложенной под бок. Десять лет спустя он сообщил об опыте 557 последовательных чрескожных нефроскопий, выполненных через такой доступ [23,24]. Он описал хирургические и анестезиологические преимущества методики, но несмотря на это она не стала общепринятой и остается дополнительным методом. На самом деле, немногие авторы сообщили о результатах применения такого положения больного в повседневной клинической практике [4,22–24,26].
Таким образом, целью настоящей статьи было детальное описание модифицированного по Galdakao положения Valdivia, которое обе группы использовали в последние годы более чем у 160 пациентов под общей анестезией для сложных эндоурологических пособий, вместе с техникой чрескожной пункции и доступа к полостной системе почки в этом положении. Эта модификация положения Valdivia на спине включае модифицированное литотомическое положение [27], позволяющее использование одновременного ретроградного и чрескожного доступа к мочевым путем и сохраняющее все хирургические и анестезиологические преимущества прежнего положения Valdivia.
Преимущества модифицированного по Galdakao положения Valdivia включают большую универсальность для манипуляций с камнями на всем протяжении верхних мочевых путей, принимая во внимание все большее использование комбинированного или последовательного ретроградного и чрескожного доступа к мочевым путям с использованием как ригидных, так и гибких инструментов. При этом нет необходимости менять положение больного, кроме того, положение обуславливает возможность лучшего нисходящего дренирования и извлечения фрагментов при ЧНЛТ, ослабление напряжения мочевых путей, большее пространство для инструментов и движений хирурга, меньшую лучевую нагрузку как для пациента, так и для рук хирурга. Целью является разрешение в один этап пособия при сложных формах нефролитиаза (коралловидные и крупные камни, или множественных камни почки и мочеточника) и других заболевания, таких как стриктуры мочеточника и стенозы уретеронеоцистоанастомозов. Также положения является оптимальным для пособий при стенозе уретероилеоанастомозов у больных с отведением мочи по Бриккеру или в толстокишечный кондуит. Естественно, необходимо проспективное рандомизированное исследование, сравнивающее положение на животе и на спине в плане урологических исходов (частота клиренса конкрементов, число эндоурологических пособие, ятрогенные осложнения, непосредственно связанные с пособие, такие как артериовенозные или мочевые свищи, кровотечение или повреждение внутренних органов).
Как и в случае с исходным положением Valdivia, в модифицированном по Galdakao положении Valdivia увеличивает гипермобильность почки по сравнению с положением на животе. Тем не менее, почка распологается ближе к поверхности тела. Не было отмечено ни одного случая повреждения ободочной кишки в обоих положениях на спине. Анестезиологические за и против: так как заболевание, по поводу которого предпринимается пособие (нефролитиаз или стенозы), является в большинстве случаев доброкачественным, даже маленькая вероятность серьезных кратковременных и долговременным осложнений неприемлема, особенно когда простое изменение интраоперационного положение может быть достаточно, чтобы их избежать. Большинство сердечно-сосудистых и легочных нарушений, обусловлены положением на животе, например удлинение времени пособия, нейроэндокринные и фармакокинетические эффекты (особенно заметные у больных с морбидным ожирением, кифизом и ослабленных больных), проблемы со зрением и неврологические нарушения (такие как паралич плечевого сплетения и миелопатии, вызывающие параплегию), могут быть устранены при повороте пациента на спину [12–22]. При этом могут иметь место небольшие недостатки, включая боль в спине в послеоперационном периоде, возможность повреждения связок колена либо лучевого и локтевого нервов, если верхние и нижние конечности неправильно защищены и уложены, и респираторные эффекты, происходящие из-за прогрессивного краниального смещение диафрагмы под общей анестезией.
Источник: Focus on Details. Supine Valdivia and modified lithotomy position for simultaneous anterograde and retrograde endourological access. THE AUTHORS JOURNAL COMPILATION, BJ U I NTERNATIONAL 2007
Авторы: Gaspar Ibarluzea, Cesare M. Scoffone, Cecilia M. Cracco, Massimiliano Poggio, Francesco Porpiglia, Carlo Terrone†, Ander Astobieta, Isabel Camargo, Mikel Gamarra, Augusto Tempia, Josè G. Valdivia Uria and Roberto Mario Scarpa. Department of Urology, Galdakao Hospital, Bizkaia, Basque Country, Spain
Перевод: к.м.н. Матюхов Игорь Павлович, асп. Георгий Альбертович Восканян. НИИ Уронефрологии и репродуктивного здоровья человека Первый МГМУ им. И.М. Сеченова
1 — Goodwin WE, Casey WC, Woolf W. Percutaneous trocar (needle) nephrostomy in hydronephrosis. J Am Med Assoc 1988; 157: 891–4
2 — Fernstrom I, Johansson B. Percutaneous pyelolithotomy, a new extraction technique. Scand J Urol Nephrol 1976; 10: 257–9
3 — Alken P, Hutschenreiter G, Gunther R, Marberger M. Percutaneous stone manipulation. J Urol 1981; 125: 463–6
4 — Ng MT, Sun WH, Cheng CW, Chang ES. Supine position is safe and effective for percutaneous nephrolithotomy. J Endourol 2004; 18: 469–74
5 — Clayman RV, Bub P, Haaff E, Dresner S. Prone flexible cystoscopy: an adjunct to percutaneous stone removal. J Urol 1987; 137: 65–7
6 — Leal JJ. Percutaneous removal of renal and ureteral stones with and without concomitant transurethral manipulation by a urologist using anterograde and retrograde techniques without a radiologist’s assistance. J Urol 1988; 139: 1184–7
7 — Lehman T, Bagley DH. Reverse lithotomy modified prone position for simultaneous nephroscopic and ureteroscopic procedures in women. Urology 1988; 32: 529–31
8 — Scarpa RM, Cossu FM, De Lisa A, Porru D, Usai E. Severe recurrent ureteral stricture. the combined use of an anterograde and retrograde approach in the prone split-leg position without X-rays. Eur Urol 1997; 31: 254–6
9 — Grasso M, Nord R, Bagley DH. Prone split leg and flank roll positioning: simultaneous anterograde and retrograde access to the upper urinary tract. J Endourol 1993; 7: 307–10
10 -Kerbl K, Clayman RV, Chandhoke PS, Urban DA, De Leo BC, Carbone JM. Percutaneous stone removal with the patient in a flank position. J Urol 1994; 151: 686–8
11 — Landman J, Venkatesh R, Lee DI et al. Combined percutaneous and retrograde approach to staghorn calculi with application of the ureteral access sheath to facilitate percutaneous nephrolithotomy. J Urol 2003; 169: 64–7
12 — Cheng MA, Todorov A, Tempelhoff R, McHugh T, Crowder CM, Lauryssen C. The effect of prone positioning on intraocular pressure in anesthetized patients. Anaesthesiology 2001; 95: 1351–5
13 — Anderton JM, Schady W, Markham DE. An unusual cause of postoperative brachial plexus palsy. Br J Anaesth 1994;
14 — Anderton JM. The prone position for the surgical patient: a historical review of the principles and hazards. Br J Anaesth 1991; 67: 452–63
15 — Mahajan RP, Hennessy N, Aitkenhead AR, Jellinek D. Effect of three different surgical prone positions on lung Volumes in healthy volunteers. Anaesthesia 1994; 49: 583–6
16 — Bhardwaj A, Long DM, Ducker TB, Toung TJ. Neurologic deficits after cervical laminectomy in the prone position. J Neurosurg Anesthesiol 2001; 13: 314–9
17 — Pump B, Talleruphuus U, Christensen NJ, Warberg J, Norsk P. Effects of supine, prone, and lateral positions on cardiovascular and renal variables in humans. Am J Physiol Regul Integr Comp Physiol 2002; 283: R174–80
18 — Schou M, Pump B, Gabrielsen A et al. Cardiovascular and neuroendocrine responses to left lateral position in non- obese young males. J Gravit Physiol 2001; 8: 15–9
19 — Takizawa D, Hiraoka H, Nakamura K, Yamamoto K, Horiuchi R. Influence of the prone position on propofol pharmacokinetics. Anaesthesia 2004; 59: 1250–1
20 — Tiefenthaler W, Gabl M, Teuchner B, Benzer A. Intraocular pressure during lumbar disc surgery in the knee-elbow position. Anaesthesia 2005; 60: 878–81
21 — Gofrit ON, Shapiro A, Donchin Y et al. Lateral decubitus position for percutaneous nephrolithotripsy in the morbidly obese or kyphotic patieny. J Endourol 2002; 16: 383–6
22 — Frattini A, Salsi P, Ferretti S, Ciuffreda M, Cortellini P. Percutaneous nephrolithotripsy (PCNL) in supine position: our experience. Eur Urol Suppl
23 — Valdivia Uria JG, Valle Gerhold J, Lopez Lopez JA et al. Technique and complications of percutaneous nephroscopy: experience with 557 patients in the supine position. J Urol 1998; 160: 1975–8
24 — Valdivia Uria JG, Valle J, Villarroya S. Why is percutaneous nephroscopy still performed with patient prone? J Endourol 1990; 4: 269–72
25 — Barbaric ZL, Hall T, Cochran ST, Heitz DR, Schwartz RA, Krasny RM. Percutaneous nephrostomy. placement under CT and fluoroscopy guidance. AJR Am J Roentgenol 1997; 169: 151–5
26 — Shoma AM, Eraky I, El-Kenawy MR, El-Kappany HA. Percutaneous nephrolithotomy in the supine position. technical aspects and functional outcome compared with the prone technique. Urology 2002; 60: 388–92
27 — Ibarluzea G, Gamarra, M.Gallego JA. Percutaneous kidney lithotripsy. Clinical course, indications and current methodology in our lithotripsy unit. Arch Esp Urol 2001; 54: 951–69
Correspondence: Cesare M. Scoffone, Clinica Urologica, Università di Torino, Ospedale San Luigi, Regione Gonzole, 10, 10043 Orbassano (Torino), Italy.
Читайте также:
